Tuy nhiên, hầu hết bệnh nhân HCC đều ở giai đoạn từ giữa đến cuối khi được chẩn đoán lần đầu và mất cơ hội chữa khỏi bệnh triệt để như phẫu thuật và ghép gan. Do đó, việc khám phá các lựa chọn điều trị toàn thân hiệu quả có ý nghĩa rất lớn trong việc cải thiện tiên lượng chung của bệnh nhân HCC.
Trong những năm gần đây, các lựa chọn điều trị toàn thân cho HCC đã có những tiến bộ đáng kể, không chỉ cải thiện khả năng sống sót chung của bệnh nhân mà còn mang lại hy vọng mới cho những bệnh nhân mắc HCC giai đoạn trung bình và tiến triển. Gần đây, Giáo sư Yuan Zhengang từ Bệnh viện của Đại học Y Hải quân đã chia sẻ một báo cáo xuất sắc về "Thực trạng và suy nghĩ về điều trị toàn thân đối với ung thư biểu mô tế bào gan" tôi sẽ biên tập soạn lại báo cáo thành một tài liệu để phục vụ độc giả.
I. Tổng quan
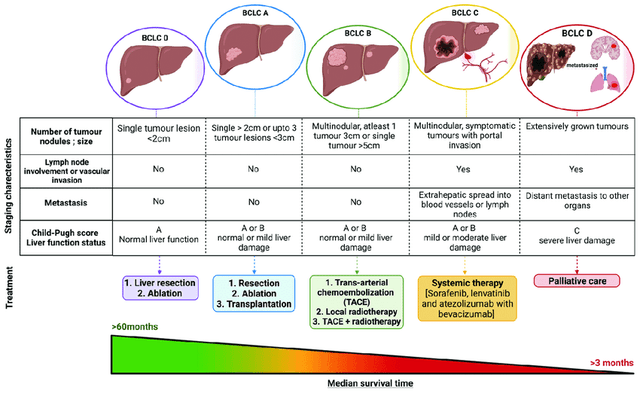
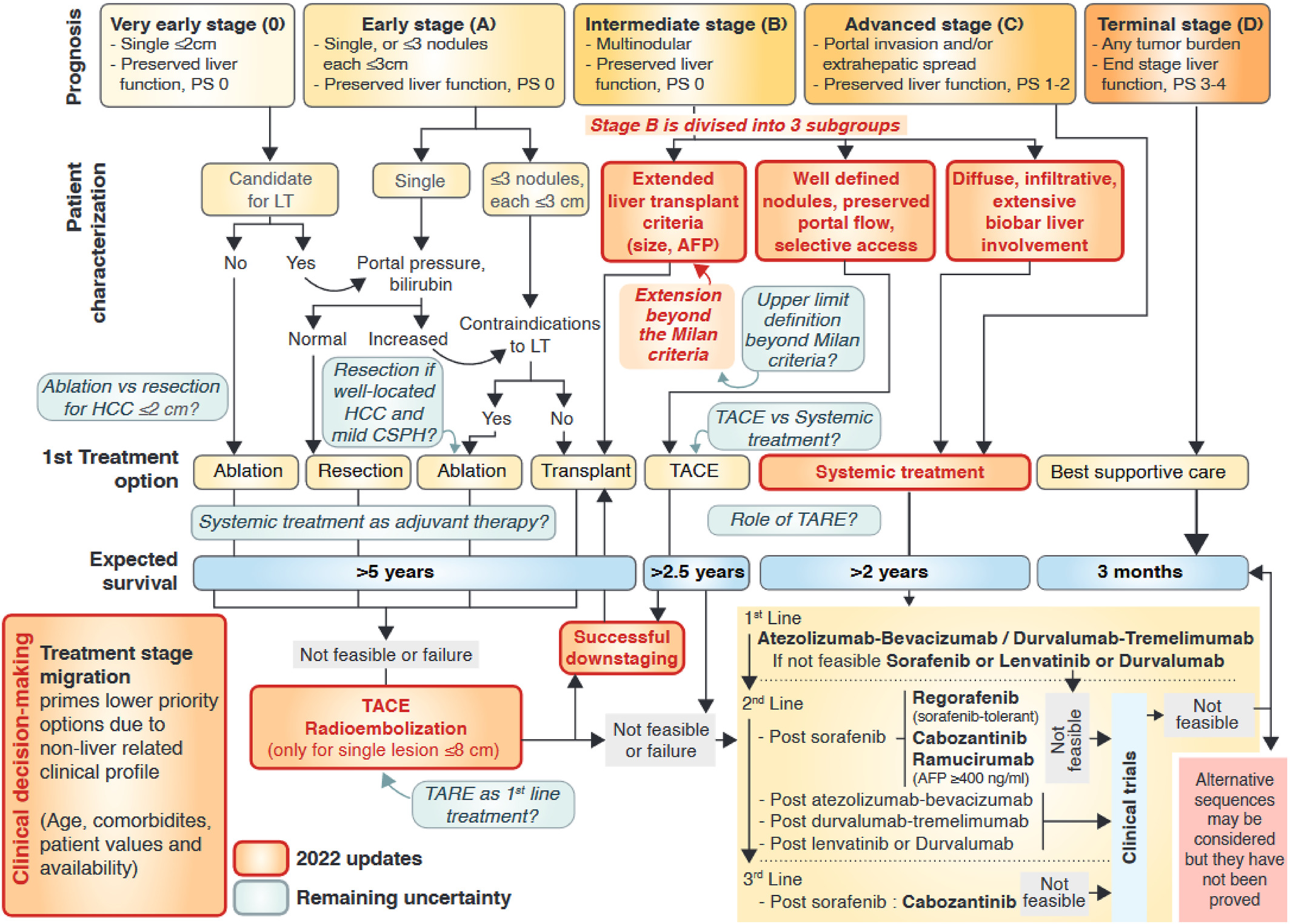
Trong những năm gần đây, liệu pháp nhắm mục tiêu và miễn dịch đối với ung thư biểu mô tế bào gan đã phát triển nhanh chóng. Những tiến bộ vượt bậc trong liệu pháp toàn thân đã mang lại những cơ hội mới cho việc điều trị bệnh nhân ung thư biểu mô tế bào gan ở các giai đoạn khác nhau. Hướng dẫn ở nhiều quốc gia khác nhau liên tục được cập nhật. Lộ trình điều trị và phân giai đoạn lâm sàng của bệnh ung thư gan được đề xuất trong "Hướng dẫn chẩn đoán và điều trị ung thư gan nguyên phát năm 2024" được thể hiện trong Hình 1. Chiến lược điều trị ung thư biểu mô tế bào gan được hướng dẫn theo giai đoạn BCLC cũng đã thay đổi. Trước đây, điều trị bằng thuốc không được khuyến cáo cho bệnh nhân mắc BCLC giai đoạn B. Bắt đầu từ năm 2023, việc điều trị bằng thuốc cũng có thể được bắt đầu đối với HCC BCLC giai đoạn B với sự phân bố lan tỏa.
Hình 1. Lộ trình phân giai đoạn lâm sàng và điều trị ung thư gan
II. Liệu pháp miễn dịch đích đầu tiên có thể cải thiện được bao nhiêu cho bệnh ung thư gan tiến triển?
1. Mô hình miễn dịch kết hợp đã trở thành phương pháp điều trị ưu tiên hàng đầu
➤ TKI: Ưu điểm là tác dụng nhanh và ORR tương đối cao. Nghiên cứu RECIST 1.1 cho thấy ORR là 18,8% và nghiên cứu mRECIST cho thấy ORR là 21,5%. Hạn chế của TKI là dễ bị kháng thuốc, thời gian hiệu quả ngắn và khó kiểm soát diễn biến của bệnh.
➤ IO: Ưu điểm là sống sót kéo dài và an toàn tốt. Nghiên cứu CheckMate 459, nghiên cứu KEYNOTE 224 và rationaLE-301 cho thấy hệ điều hành của nó có thể đạt lần lượt 16,4 tháng, 17 tháng và 15,9 tháng. Hạn chế là nó không có lợi thế về ORR so với TKI.
➤ Đột phá chung: Giúp bệnh nhân sống sót tốt hơn và hiệu quả cao hơn. Sự kết hợp miễn dịch mục tiêu là phương pháp điều trị tiêu chuẩn hiện nay.
1) Nghiên cứu IMbrave150
Nghiên cứu IMbrave150 là một nghiên cứu lâm sàng giai đoạn III, đa trung tâm, có đối chứng ngẫu nhiên, ngẫu nhiên, có đối chứng. Bệnh nhân HCC được chọn ngẫu nhiên theo tỷ lệ 2:1 để nhận liệu pháp kết hợp atezolizumab (1200 mg IV q3w) + bevacizumab (15 mg/kg IV q3w) (T+A) hoặc sorafenib (400 mg PO BID) cho đến khi không có lợi ích lâm sàng hoặc xảy ra độc tính không thể chấp nhận được. Các tiêu chí chính là OS và PFS trong nhóm bệnh nhân có chủ đích điều trị (ITT). Tiêu chí phụ là tỷ lệ đáp ứng khách quan (ORR) và thời gian đáp ứng (DoR).
Dữ liệu được công bố vào năm 2022 [1] cho thấy mOS của phác đồ T+A là 19,2 tháng và mOS của nhóm sorafenib là 13,4 tháng. Phác đồ T+A có thể giảm 34% nguy cơ hệ điều hành (HR=0,66). KTC 95% 0,52-0,85, P<0,001). mPFS của phác đồ T+A là 6,9 tháng, tốt hơn so với 4,3 tháng của nhóm sorafenib và nguy cơ tiến triển bệnh giảm 35% (HR=0,65, KTC 95% 0,53-0,81, P<0,001 ). Việc áp dụng rộng rãi phác đồ T+A cũng thu hút sự chú ý của chúng tôi đến vấn đề xuất huyết do giãn tĩnh mạch thực quản. Phân tích phân nhóm xâm lấn mạch máu lớn của nghiên cứu IMbrave150 cho thấy điều trị T+A có liên quan đến việc tăng tỷ lệ xuất huyết do giãn tĩnh mạch (14%) và xuất huyết tiêu hóa (5%), đặc biệt ở những bệnh nhân bị giãn tĩnh mạch thực quản.
2) Nghiên cứu về HIMALAYA
Nghiên cứu HIMALAYA là nghiên cứu Giai đoạn III ngẫu nhiên, nhãn mở, đa trung tâm, toàn cầu. Từ tháng 10 năm 2017 đến tháng 6 năm 2019, 1950 bệnh nhân đã được sàng lọc tại 181 địa điểm ở 16 quốc gia. Tiêu chí chọn bệnh nhân là: HCC không thể cắt bỏ, BCLC giai đoạn B và C, không có liệu pháp điều trị toàn thân trước đó, Không phù hợp với điều trị tại chỗ, điểm Child Pugh A, và không có huyết khối ở tĩnh mạch cửa chính.
1171 bệnh nhân được chia ngẫu nhiên thành ba nhóm: nhóm STERID (393 trường hợp), nhóm durvalumab (389 trường hợp) và nhóm sorafenib (389 trường hợp). Nhóm STERID: Thêm một liều tremelimumab 300 mg vào điều trị thông thường 1.500 mg durvalumab 4 tuần một lần; Nhóm STERID: 1.500 mg durvalumab dưới dạng đơn trị liệu, 4 tuần một lần; Nhóm Sorafenib: 400 mg, hai lần một ngày.
Kết quả nghiên cứu cho thấy thời gian sống thêm trung bình của nhóm STERID là 16,43 tháng, của nhóm durvalumab là 16,56 tháng và của nhóm sorafenib là 13,77 tháng. Tỷ lệ sống sót sau 36 tháng lần lượt là 30,7%, 24,7% và 20,2%. Tỷ lệ đáp ứng khách quan (ORR) do điều tra viên đánh giá của nhóm STRIDE, nhóm durvalumab và nhóm sorafenib lần lượt là: 20,1%, 17,0% và 5,1%. Thời gian tiến triển bệnh trung bình của ba nhóm là: 5,4 tháng, 3,8 tháng và 5,6 tháng [2]. Ưu điểm là không cần quan tâm đến nguy cơ chảy máu do giãn tĩnh mạch thực quản.
Trong dữ liệu cập nhật theo dõi hệ điều hành 4 năm [3], tỷ lệ sống sót chung (OS) 4 năm của nhóm phác đồ STRIDE là 25,2%, cao hơn 67% so với nhóm sorafenib (25,2% so với 15,1%). Trong số những bệnh nhân đã kiểm soát được bệnh, tỷ lệ sống sót sau 4 năm của nhóm điều trị STRIDE là 36,2%, cao hơn 78% so với nhóm sorafenib (36,2% so với 20,3%).
3) Nghiên cứu CheckMate-9DW
CheckMate-9DW là một thử nghiệm lâm sàng đa trung tâm, ngẫu nhiên, nhãn mở, toàn cầu, giai đoạn III lớn so sánh nivolumab và ipilimumab (O+Y) ở những bệnh nhân mắc HCC tiến triển chưa được điều trị toàn thân bằng lenvatinib hoặc sorafenib.
Kết quả nghiên cứu cho thấy thời gian sống thêm trung bình của bệnh nhân ở nhóm O+Y là 23,7 tháng và thời gian sống thêm trung bình của bệnh nhân ở nhóm dùng lenvatinib hoặc sorafenib là 20,6 tháng (HR 0,79, P = 0,018). Sau thời gian theo dõi trung bình là 35,2 tháng, thời gian sống sót trung bình của nhóm O+Y là 23,7 tháng và của nhóm đối chứng là 20,6 tháng. Có sự cải thiện đáng kể ở nhóm O+Y (HR=0,79; 95%). KTC: 0,65-0,96; P = 0,0180). Tỷ lệ sống sót sau 24 tháng của hai nhóm lần lượt là 49% và 39%, tỷ lệ sống sót sau 36 tháng lần lượt là 38% và 24%, và ORR lần lượt là 36% và 13%. Tuy nhiên, PFS trung bình của hai nhóm bệnh nhân lần lượt là 9,1 tháng và 9,2 tháng và sự khác biệt không có ý nghĩa thống kê [4].
4) Nghiên cứu-312
Nghiên cứu COSMIC-312 [5] là nghiên cứu giai đoạn III ngẫu nhiên, nhãn mở. Những người tham gia được chỉ định ngẫu nhiên vào ba nhóm (2:1:1) để nhận riêng Cabozantinib cộng với atezolizumab, sorafenib hoặc Cabozantinib. Nghiên cứu cho thấy mặc dù PFS của Cabozantinib kết hợp với atezolizumab tốt hơn so với nhóm sorafenib, nhưng không có sự khác biệt đáng kể về OS giữa hai nhóm khi phân tích tạm thời.
5) CARES-310
Nghiên cứu CARES-310 là một nghiên cứu lâm sàng giai đoạn III ngẫu nhiên, có đối chứng, đa trung tâm quốc tế, bao gồm tổng cộng 543 bệnh nhân mắc ung thư biểu mô tế bào gan di căn hoặc không thể cắt bỏ, chưa được điều trị toàn thân trước đó. Họ được chọn ngẫu nhiên theo tỷ lệ 1:1 để nhận Carreli. Tizumab kết hợp với điều trị bằng apatinib (kết hợp Ai kép) (272 trường hợp) hoặc điều trị bằng sorafenib (271 trường hợp), kết quả cuối cùng chính là PFS và OS. Kết quả cho thấy [6] so với nhóm điều trị tiêu chuẩn, thời gian sống thêm trung bình của nhóm điều trị "Double Ai" dài hơn đáng kể (22,1 tháng so với 15,2 tháng; HR=0,62, 95%CI: 0,49-0,80; một- hai bên p<0,0001). Sau 16 tháng theo dõi sâu hơn, phân tích cuối cùng cho thấy thời gian sống thêm trung bình của nhóm "AIDS kép" đạt 23,8 tháng, dài hơn 8,6 tháng so với nhóm điều trị chuẩn (23,8 tháng so với 15,2 tháng; HR= 0,64, KTC 95%: 0,52-0,79; p<0,0001 một phía).
Có sự khác biệt về độ an toàn của các phác đồ điều trị kết hợp miễn dịch khác nhau và các phản ứng bất lợi cũng không giống nhau. Điều đáng được quan tâm là liệu bệnh nhân có chống chỉ định miễn dịch hay không và liệu anh ta có xu hướng chảy máu hay không. Hầu hết bệnh nhân chọn liệu pháp miễn dịch đích trên lâm sàng đều dựa trên hai điểm này. Tóm tắt về liệu pháp miễn dịch mục tiêu hàng đầu đối với ung thư biểu mô tế bào gan được trình bày trong Bảng 1. Hiện nay nó đã bước vào thời kỳ ổn định, với tỷ lệ hiệu quả là 20-30% và thời gian sống sót khoảng 20 tháng.
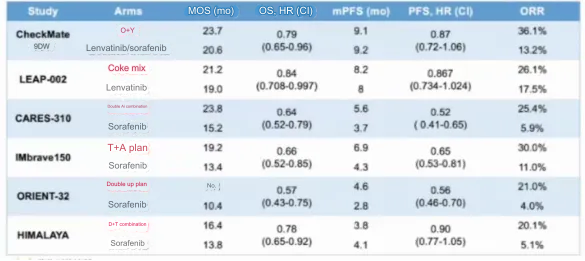
Bảng 1. Tóm tắt liệu pháp miễn dịch đích đầu tay điều trị ung thư biểu mô tế bào gan
Hiện tại, phác đồ điều trị bậc hai tối ưu cho HCC sau thuốc ức chế điểm kiểm soát miễn dịch (ICI) vẫn chưa được xác định. Kết quả của một nghiên cứu về regorafenib kết hợp với pembrolizumab đã được báo cáo tại Hội nghị thường niên ASCO năm 2024. Nghiên cứu đã xác định 2 đoàn hệ dựa trên phương pháp điều trị trước đó, đoàn hệ 1: atezolizumab + bevacizumab Đoàn hệ 2: Bất kỳ phác đồ ICI nào khác (đơn độc hoặc kết hợp), với điểm cuối chính là tỷ lệ phản hồi tổng thể (ORR) theo đánh giá trung tâm độc lập (RECIST 1.1).
Kết quả cho thấy ORR của đoàn hệ 1 là 5,9%, của đoàn hệ 2 là 11,1% và tỷ lệ bệnh ổn định lần lượt là 48,5% và 63,0%. PFS trung bình là 2,8 tháng ở nhóm 1 và 4,2 tháng ở nhóm 2. Đây là nghiên cứu tiền cứu đầu tiên đánh giá thuốc ức chế kinase + ICI sau liệu pháp ICI đầu tay. Regorafenib + pembrolizumab đã cho thấy một số hoạt động ở phác đồ bậc hai sau phác đồ ICI bậc một.
Vậy hiệu quả của việc bổ sung một số phương pháp điều trị bằng thuốc trên cơ sở liệu pháp miễn dịch đích là gì?
1) Nghiên cứu MORPHEUS-gan
Nghiên cứu về gan MORPHEUS đã đánh giá tiragolumab kết hợp với atezolizumab (atezo) và bevacizumab (bev) ở bệnh nhân ung thư biểu mô tế bào gan giai đoạn Ib/II không thể cắt bỏ, tiến triển cục bộ hoặc di căn (uHCC). Tổng cộng có 58 bệnh nhân được chia ngẫu nhiên thành các nhóm (nhóm tira+atezo+bev, n=40; atezo+bev, n=18). Kết quả nghiên cứu cho thấy thời gian theo dõi trung bình là 14,0 tháng ở nhóm tira+atezo+bev và 11,8 tháng ở nhóm đối chứng. So với nhóm đối chứng, nhóm tira+atezo+bev có ORR cao hơn (42,5% so với 11,1%); PFS dài hơn (11,1 tháng so với 4,2 tháng) và tỷ lệ nguy cơ PFS (HR) tương ứng là 0,42 (95 %). KTC: 0,22-0,82). Kết quả của nghiên cứu IMbrave152 thử nghiệm giai đoạn III rất đáng mong đợi.
2) Nghiên cứu AdvanTlG-206
AdvanTIG-206 là nghiên cứu nhãn mở ngẫu nhiên giai đoạn II về nghiên cứu ociperlimab (OCI) + tislelizumab (TIS) + BAT1706 (bevacizumab biosimilar) so với TIS + BAT1706 ở những bệnh nhân mắc ung thư biểu mô tế bào gan (HCC) tiến triển. Ở những bệnh nhân bị HCC tiến triển, TIS+BAT1706 cho thấy ORR tốt, trong khi việc bổ sung OCI vào chế độ điều trị này không làm tăng tác dụng chống ung thư. Dữ liệu hệ điều hành chưa hoàn thiện và cần được theo dõi thêm.
Ngoài việc bổ sung thuốc có thể bổ sung thêm phương pháp điều trị can thiệp được không?
Nghiên cứu LAUNCH là một nghiên cứu lâm sàng giai đoạn III ngẫu nhiên có đối chứng, đa trung tâm, nhằm đánh giá hiệu quả và độ an toàn của lenvatinib (LEN) kết hợp với TACE so với LEN đơn thuần trong điều trị bước đầu cho bệnh HCC tiến triển. Kết quả nghiên cứu cho thấy rằng trong hệ điều hành điểm cuối chính (trung vị 17,8m so với 11,5m, HR=0,45; P<0,001) và các điểm cuối khác PFS (trung vị 10,6m so với 6,4m HR=0,43; P<0,001), Trong ORR (54,1% so với 25,0%; P <0,001) và trong mỗi phân tích nhóm nhỏ, lợi ích của LEN+TACE rõ ràng hơn so với chỉ dùng LEN.
III. Điều trị tiếp theo bằng liệu pháp miễn dịch đích ung thư gan
Ở giai đoạn này, có những thách thức lớn trong việc lựa chọn phương pháp điều trị bậc hai cho HCC và chiến lược lựa chọn bậc hai dựa trên mô hình bậc một vẫn cần được hỗ trợ bởi bằng chứng y tế dựa trên bằng chứng cấp cao. Có dữ liệu tương đối phong phú về những bệnh nhân đã tiến triển khi dùng sorafenib trong liệu pháp hệ thống bậc hai tiên tiến, nhưng có tương đối ít dữ liệu về những bệnh nhân đã tiến triển khi dùng lenvatinib và liệu pháp kết hợp miễn dịch đích.
1) Sau khi điều trị bằng lenvatinib, dữ liệu sống sót không tiến triển của các phương pháp điều trị tiếp theo cho thấy mPFS của sorafenib là 1,8 tháng và mPFS của regorafenib là 3,2 tháng.
2) Ipilimumab kết hợp với nivolumab/pembrolizumab, như một liệu pháp cấp cứu sau khi điều trị bằng IO, cho thấy hoạt động chống khối u lâu dài và mang lại lợi ích sống còn đáng khích lệ.
3) So sánh các phác đồ đơn trị liệu TKI sau quá trình điều trị T+A cho thấy mPFS của lenvatinib tốt hơn đáng kể so với sorafenib và mOS tương đương. Một số bệnh nhân cũng có thể được hưởng lợi từ việc duy trì điều trị hiện tại.
4) Nghiên cứu IMbrave251 là nghiên cứu so sánh atezolizumab kết hợp với lenvatinib/sorafenib với lenvatinib đơn thuần hoặc sorafenib ở những bệnh nhân mắc HCC không thể cắt bỏ trước đây đã nhận được chế độ điều trị T+A. Nghiên cứu ngẫu nhiên, nhãn mở, giai đoạn III về đơn trị liệu bằng không được cho là có tác dụng. cung cấp những lời khuyên tốt cho việc điều trị chéo bằng liệu pháp miễn dịch.
4. Điều trị bổ trợ sau phẫu thuật ung thư gan
Điều trị bổ trợ là một biện pháp quan trọng để giảm nguy cơ tái phát HCC sau phẫu thuật và kéo dài thời gian sống sót. Sự đồng thuận hiện nay là đối với bệnh nhân ung thư gan nhiễm HBV, điều trị bằng thuốc kháng virus sau phẫu thuật có thể làm giảm đáng kể sự tái phát và kéo dài thời gian sống sót. Ngoài ra, vẫn chưa có kết luận cuối cùng về việc nên lựa chọn phương pháp điều trị bổ trợ nào sau phẫu thuật ung thư gan và thời gian điều trị sẽ kéo dài bao lâu. Điều trị bổ trợ cho bệnh nhân có nguy cơ cao sau phẫu thuật cần được khám phá.
5. Thăm dò dấu ấn sinh học ung thư gan
Hướng phát triển trong tương lai của liệu pháp hệ thống là khám phá các dấu ấn sinh học. Hiện tại không có dấu ấn sinh học dự đoán tác dụng chữa bệnh/tiên lượng nào được công nhận đối với HCC. Nghiên cứu chẩn đoán và điều trị chính xác ung thư gan ở cấp độ bệnh lý phân tử cần được tăng cường. Chỉ bằng cách tìm kiếm các dấu hiệu phân tử khối u cụ thể và lựa chọn các nhóm nhạy cảm, về cơ bản chúng ta mới có thể đạt được phương pháp điều trị phù hợp và cá nhân hóa.
6. Tóm tắt
Điều trị ung thư gan gặp nhiều thách thức ở giai đoạn này
● Câu đầu tiên: Làm thế nào để chọn giải pháp tốt nhất để mang lại cơ hội sống sót lâu dài cho nhiều bệnh nhân hơn?
● Câu thứ hai: Thời điểm chuyển đổi điều trị và lựa chọn kế hoạch tuần tự?
● Hỗ trợ sau mổ: Sàng lọc bệnh nhân như thế nào?
Trong kỷ nguyên của liệu pháp miễn dịch đích, liệu pháp nhắm mục tiêu và thuốc trị liệu miễn dịch cũng như các chương trình kết hợp miễn dịch đích mang lại nhiều cơ hội hơn cho bệnh ung thư gan.
● Liệu pháp kết hợp miễn dịch đã trở thành một trong những tiêu chuẩn điều trị hàng đầu mới cho bệnh ung thư gan tiến triển. Tuy nhiên, ung thư gan rất không đồng nhất và phác đồ kết hợp miễn dịch tối ưu cần được nghiên cứu thêm.
● Cách chọn giải pháp tuyến hai và tuyến sau đòi hỏi phải tìm hiểu thêm. Các nghiên cứu gợi ý rằng việc tiếp tục nhận liệu pháp miễn dịch sau khi tiến triển liệu pháp miễn dịch bậc một vẫn có cơ hội đạt được lợi ích lâm sàng.
● Nghiên cứu về liệu pháp bổ trợ sau phẫu thuật đang được tiến hành nhưng phác đồ và đối tượng tối ưu vẫn chưa được xác định.
● Việc khám phá các dấu ấn sinh học để dự đoán hiệu quả/tiên lượng HCC đang ngày càng phát triển và sự kết hợp dấu ấn sinh học, thuật toán/mô hình dự đoán tiên lượng, v.v. được kỳ vọng sẽ trở thành hướng nghiên cứu trong tương lai.
Nguồn:
1. Cheng AL, Qin S, Ikeda M, Galle PR, Ducreux M, Kim TY, et al. Updated efficacy and safety data from IMbrave150: Atezolizumab plus bevacizumab vs. sorafenib for unresectable hepatocellular carcinoma. J Hepatol 2022; 76(4):862-873.
2. Abou-Alfa GK, Lau G, Kudo M, Chan SL, Kelley RK, Furuse J, et al. Tremelimumab plus Durvalumab in Unresectable Hepatocellular Carcinoma. NEJM Evid 2022; 1(8):EVIDoa2100070.
3. Bruno S SL, Robin KK, et al.Four-year overall survival update from the phase 3 HIMALAYA study of tremelimumab plus durvalumab in unresectable hepatocellular carcinoma.2023 WCGIC.Abstract SO-15.
4. Peter Robert Galle eaNNpiIvlLosSaf-ltfuhcu.
5. Yau T, Kaseb A, Cheng AL, Qin S, Zhu AX, Chan SL, et al. Cabozantinib plus atezolizumab versus sorafenib for advanced hepatocellular carcinoma (COSMIC-312): final results of a randomised phase 3 study. Lancet Gastroenterol Hepatol 2024; 9(4):310-322.
6. Qin S CS, Gu S, et al. Camrelizumab plus rivoceranib versus sorafenib as first-line therapy for unresectable hepatocellular carcinoma (CARES-310): a randomised, open-label, international phase 3 study[J]. Lancet, 2023, 402(10408):1133-1146.
Xơ gan là một bệnh gan mạn tính tiến triển do một hoặc nhiều nguyên nhân gây ra và có đặc điểm mô học là xơ hóa lan tỏa, giả tiểu thùy và các nốt tái tạo trong mô gan.

Lâu nay, nhắc tới côn trùng có thể khiến nhiều người phải ngứa da đầu. Tuy nhiên, côn trùng giờ đây đã trở thành món ăn được yêu thích mới trên bàn ăn và là nguồn thực phẩm mới nổi.

Ung thư gan là một trong những loại ung thư phổ biến nhất ở nước tôi. Nó có khởi phát âm thầm và không có biểu hiện lâm sàng rõ ràng ở giai đoạn đầu. Chúng ta thường gọi gan là “cơ quan thầm lặng”.

Vào ngày 18 tháng 5 năm 2024, "Hội nghị học thuật điều trị lâm sàng bệnh viêm gan B mãn tính lần thứ sáu" tập trung vào việc điều trị lâm sàng bệnh viêm gan B mãn tính đã được tổ chức hoành tráng tại Hạ Môn.

Hội nghị thường niên của Hiệp hội Nghiên cứu Gan Châu Âu (EASL) năm 2024 sẽ được tổ chức tại Milan, Ý, từ ngày 5 đến ngày 8 tháng 6 năm 2024. Tôi sẽ chia sẻ nội dung quan trọng có liên quan.

Ung thư gan là một khối u ác tính xảy ra ở gan. Nó được chia thành nguyên phát và thứ phát. Hôm nay chúng ta sẽ nói về ung thư gan nguyên phát, là những khối u ác tính có nguồn gốc từ tế bào gan và tế bào biểu mô ống mật trong gan.
.jpeg&w=640&q=75)
Rau mang lại màu sắc và chất dinh dưỡng phong phú cho bữa ăn của chúng ta và luôn được công nhận là thực phẩm lành mạnh từ khi còn nhỏ chúng ta đã được giáo dục nên ăn nhiều trái cây và rau quả nhưng ít người biết rằng không phải loại rau nào cũng tốt.

Trung Quốc là nước có tỷ lệ mắc ung thư biểu mô tế bào gan (HCC) cao và phương pháp điều trị bằng phẫu thuật chủ yếu được sử dụng cho HCC giai đoạn đầu.